什麼是未來現代醫療發展趨勢?透過個人化健康檢查的疾病預防,加上大數據分析的健康風險控管,精準醫療逐漸為健康管理產業帶來轉變。康聯集團透過旗下康聯生醫發展新一代健康管理平台,以數據為核心推出個人化智慧健康之應用,期望透過新科技,帶給民眾更好的健康管理利器。
#基因檢測
在精準醫療的時代,透過個人化健康檢查的疾病預防,加上大數據分析的健康風險控管,是現代醫療發展的大勢所趨。康聯集團透過旗下康聯生醫發展新一代健康管理平台,以數據為核心推出個人化智慧健康之應用,期望透過新科技,帶給民眾更好的健康管理利器。 以往在疾病預防的觀念上,都是聯想到健康檢查,而「數位健康」在個人化的健康管理上為何扮演如此重要角色?康聯生醫科技股份有限公司董事長林群倫表示,民眾以往都是有了疾病才看醫生,健康管理的概念是要在疾病發生之前做好慢性疾病或者體重、睡眠等管理等來避免疾病發生。 林群倫說明,「數位健康」有個很重要的環節,那就是數據分析,透過每年健檢報告的數據歷史軌跡,以往能做「健康風險評估」,現在,更能制定個人化的健康管理方案。。 智慧化Call Center與個人化健康管理平台 來精準評估風險 以能快速掌握身體問題的第一層防護的健檢來說,有別傳統模組,康聯著重於針對個人健康狀況、量身定制的檢查方案,在現代大多數人處於「亞健康」的狀態下,從慢性疾病、營養攝取,以及與生活息息相關的睡眠問題等切入,提早預防疾病風險。 康聯以先進之健康數據分析技術,針對每位嘉賓長年累積之各項健康資料,快速評估狀況並建議最適化之健檢方案,除每年常規之健檢服務外,在後疫情時代,透過專業健管師諮詢輔以智慧化聊天機器人,可更有效快速地量身訂製健康管理方案。 以好發慢性疾病風險來說,除了亞健康疾病如體重管理、慢性病、睡眠問題等解決方案,康聯更連結國內外知名產學研團隊,帶入專屬亞洲聲紋數據與學研實驗室獨家演算法開發,透過醫師顧問群與醫院臨床驗證,走向多種呼吸相關適應症之數位療法應用。 康聯於投入生醫領域應用之研發,透過蒐集海量、精準的醫事檢測資料,以數據科技為核心,提升精準檢測,將推出客製化健康風險分析與管理方案,提供民眾最佳疾病預防選擇。另外,在促進健康的各項環節中,亦著重於營養、運動、舒壓、睡眠四大面向,協助民眾擬定個人化的健康促進方案。 客製化數位健康管理方案 有效控管疾病 林群倫認為,「每個人都值得最適合自己的數位健康管理方案」,這需要仰賴專業的團隊與醫療數據科技。以同樣康聯集團旗下的康誠、康儀來說,康誠所提供的基因檢測服務,像是對於國人威脅的最大的---癌症遺傳性基因檢測,提供癌症精準醫療用藥指引,以及用藥預後分析、復發追蹤,目前更著手規劃建立亞太檢測中心,致力縮短檢測時間與降低民眾費用負擔。 集團旗下康儀科技提供醫學檢驗設備之銷售與服務,協助專業人士提升服務流程與品質。現今康儀已成為國內集設備耗材代理銷售、技術服務與物流運輸於一體的佼佼者,將持續進行研發與創新,投入微生物臨床技術、檢驗流程、冷鏈儲運等領域,提供最全面的產品與服務。 康聯集團整合旗下的健康服務內容,打造健康生態圈,在精準醫療的趨勢之下,透過運用大數據與健康風險評估,系統化健康分級與智能健康個人管理,提供最務實且長期的健康管理解決方案。 康聯集團以結合科技、跨領域智慧,專業的健康風險評估、健康管理諮詢等服務核心,並根據個人化的遺傳、環境、生活等資訊來量身客製健康管理方案。林群倫強調,在健康管理的具體發展上,目前康聯正研發的個人化的睡眠聲波分析搭配手機的便利方式,為現代人最重要的睡眠等問題來做監測並找出解決方案,在智慧醫療方面,則會整合醫師、營養師等提供最佳疾病解決方法。康聯期望透過這樣多元科技、數據,與臨床醫學的整合,成為全球健康服務生態圈的領航者,協助民眾真正達到健康永續的最終目標。
(優活健康網記者馮逸華/採訪報導)肺癌年年蟬聯國人癌症致死率之首,但你知道其實肺癌也有分不同種類嗎?依肺癌依生物特性和臨床表現,可分為「非小細胞癌」與「小細胞癌」,前者約佔9成,主要包括鱗狀上皮細胞癌、肺腺癌、大細胞癌;後者則常發生在呼吸道中央,因為生長快速、容易轉移,治癒率多半較低。因此在治療肺癌前,臨床多建議以次世代基因定序(NGS)檢測,一次性找出不同的致病基因,才能有效掌握肺癌黃金治療期,並制定相應的治療策略。肺癌突變基因EGFR佔半數 MET存活期最短新光醫院醫療副院長高尚志指出,今日肺癌已進入精準醫療世代,「非小細胞肺癌」是最常見的肺癌種類,有一些已知的致病基因突變,以EGFR基因佔半數以上最為常見,其他還包括ALK、BRAF、ROS1、MET等基因突變型別。「肺癌EMBA」包括:E = EGFR,在一般晚期肺腺癌患者中佔50%以上,是肺癌中最常見的基因型。M = MET,此突變基因過去只能傳統化療,但成效不佳,屬肺癌中患者存活率最短。B = BRAF,發生比率僅佔1~3%的罕見肺癌基因,由於此基因突變亦會在其他癌症中被發現,加上肺癌檢測率不高,因此許多患者會不知道自己是BRAF突變。A = ALK,在EGFR檢測陰性的患者中,約有1成的機會檢測為ALK陽性,且年輕女性與不抽菸患者佔多數。目前已有健保給付及第1、2代標靶藥物,可穩定控制病情避免惡化。1次NGS檢測就找出致病基因 大幅提高肺癌存活率過去治療肺癌時,傳統檢測多使用螢光位元雜合、免疫組織化學染色法、PCR等技術,一次僅能選擇檢驗1種基因型,不僅可能在過程就錯過黃金治療期,一旦檢體不足,還需要重新採集,亦會面臨出血與感染風險。高尚志指出,肺癌治療分秒必爭,若以NGS檢測,可以一次對幾十萬到幾百萬條核酸分子同時進行序列測定、對基因進行全貌分析,一次性找出致病罕見變異基因。患者無須擔心進行NGS檢測所費不貲,醫療團隊可依據患者的經濟狀況,提供最適切的NGS類型及建議,對抗肺癌未必帶來沉重經濟負擔。多元標靶藥物問世 罕見肺癌病友可望受惠新光醫院胸腔內科主治醫師葉育雯補充,過往因肺癌確診後多需使用化療和第1代標靶藥物治療,造成身體精力及元氣大幅衝擊,也因副作用耐受度降低,醫囑順從度大幅降低;這類患者因為治療不積極,存活期往往很短。但隨著醫療科技發展,ALK、MET等罕見肺癌型別的多元標靶藥物已接連問世,可望讓不同型別的肺癌患者皆受惠使用;在肺癌發生進展時,也有望接續替換其他標靶藥物,醫囑順從度和治療成果也與過去大相逕庭。葉育雯呼籲,目前醫師已可依據患者的用藥考量,打造客製化療程,有效提升預後患者的治療便利性、擁有更好的生活品質,建議患者應積極配合醫矚,專心與醫療團隊一起面對肺癌,就能爭取更長存活時間,累積更多人生美好記憶。延伸閱讀:患罕見肺癌6旬婦拒化療,用突破性標靶藥成功救命
(優活健康網新聞部/綜合報導)三級警戒持續延長,許多民眾擔心被傳染,即便身體出現不適症狀也不敢就醫。根據英國醫學期刊指出,癌症患者若治療延遲一個月,即可能會增加6-13%的死亡風險,且死亡風險會因延遲的時間增長。大腸直腸癌已蟬聯12年癌症發生人數之冠,常見症狀為排便習慣改變、出現血便、黏液便,以及體重減輕、貧血等。其中,血便最容易被患者誤認為痔瘡或肛裂所造成,進而忽略以致延誤治療。中國醫藥大學新竹附設醫院大腸直腸外科醫師邵彥誠說,約2-3成患者確診時已是四期,多已轉移至其他器官較難直接以手術切除。所幸,在藥物發展與進步下,現已可能透過單株抗體標靶藥物合併化療重現生機。排便習慣改變、出現血便、黏液便或體重減輕應警覺大腸直腸癌平均發生年齡約為60歲,隨著年紀的增長越要注意血便、排便習慣改變等症狀,若持續2-3周應立即就醫做進一步檢查。邵彥誠表示,抽菸、家族性遺傳、有發炎性腸道疾病史,以及曾接受放射線與免疫抑制劑治療的患者,皆為罹患大腸癌的高風險族群。此外,大腸癌與飲食習慣也有關聯,其中已開發國家的發生率較高,推測與經常食用高油脂、精緻加工與醃製等食品相關。根據國健署統計資料,第一期大腸癌治療五年存活率超過9成,第二期約8成、第三期約6成,而第四期存活率僅剩不到2成,不同分期的治療方式及預後皆會有所不同。治療前進行RAS與BRAF基因檢測 助標靶選擇以提高治療成效 邵彥誠指出,大腸癌早期患者以外科手術切除為首選,因手術治療有較大痊癒的機會,且可延長患者存活期。然而晚期或轉移性患者則以化學藥物合併標靶藥物治療的合併療法為主,因腫瘤太大或已轉移至其他器官,難以透過手術切除。晚期大腸癌患者可透過單株抗體標靶藥物合併化療進行治療。邵彥誠目前常用的單株抗體標靶藥物分別為抗血管新生(VEGF)抗體與抑制表皮細胞生長(EGFR)抗體兩種,針對左右側大腸癌有不同的成效。其中,因EGFR抗體為直接作用於表皮生長因子上,進而抑制腫瘤生長,故針對RAS與BRAF基因未突變的左側大腸癌患者,使用EGFR標靶藥物效果優於VEGF標靶藥物,因此治療前須先檢測RAS與BRAF基因是否突變。晚期大腸癌 單株抗體標靶合併化學治療提升存活期、生活品質根據大型臨床試驗證實,使用抑制表皮生長的標靶藥物合併化學治療,可顯著降低疾病惡化的風險,且無疾病惡化存活期最高達10個月,平均存活期更有可能突破兩年。邵彥誠醫師解釋,無疾病惡化存活期代表患者於追蹤期間發現腫瘤無變大或變多等現象,某種程度上可與疾病和平共處。因此,鼓勵晚期患者仍要積極面對與治療,其目的除延緩腫瘤生長與縮小,使患者有機會進行手術切除以延長壽命外,也可有效緩解症狀的不適,以提升生活品質。 邵彥誠呼籲,大腸直腸癌的治癒率相較其他癌症是較高的,患者應接受正規醫療、勿信偏方,透過多專科的醫師合作,將針對個案的特色提供精準的用藥,有效提升存活期。(文章授權提供/健康醫療網)
(優活健康網新聞部/綜合報導)在少子化的台灣,每個孩子都是寶,父母親殷切期盼孩子出世,更希望孩子能健康長大。隨著檢測技術的進步,家長們也有越來越多的選擇。最首要的是國家提供的篩檢項目,包含代謝篩檢與聽力篩檢。目前的新生兒先天性代謝異常疾病篩檢有21個項目,這些代謝疾病若未能及時治療,可能造成損害,導致永久性後遺症。禾馨醫療小兒科陳菁兒醫師指出,國民健康署提供的新生兒篩檢主要是篩檢「採檢當下」血液中的代謝產物、酵素,可以找出急性或嚴重程度較高的疾病,以便即早接受治療、減輕症狀。至於聽力篩檢,可以找出當下已經發生嚴重聽力損傷的寶寶。由政府補助的各項篩檢皆相當重要,但還是有其侷限性,陳菁兒醫師分析,所以有些未列入篩檢的疾病,或者是比較晚發病的寶寶,往往得等到出現症狀、生長遲緩時,才就醫檢查,可能錯過黃金治療期,而造成父母的自責與遺憾。受惠於醫學的進展,目前已可運用基因檢技術讓新生兒篩檢更加完善,「新生兒基因檢測」只需寶寶採取幾滴血液或是刮取口腔黏膜細胞便能進行檢驗,能夠提早驗出晚發型的寶寶,且涵蓋更多疾病種類。新生兒聽力篩檢正常,長大後卻出現聽力損傷?新生兒基因檢測的起源與聽力篩檢有關,陳菁兒醫師解釋,以往大家認為只要通過新生兒聽力篩檢的寶寶,聽力應該就沒有問題,但是後來卻發現,部分在4-5歲有語言發展遲緩的小朋友,檢查起來其實是聽力損傷造成的學習遲緩,代表仍有部分聽力損傷無法透過新生兒聽力篩檢出來。台大醫院耳鼻喉科醫師與基因醫學部團隊針對這個問題深入研究,這才發現台灣人具有一些特別常見的聽損基因及點位,於是發展出聽損基因檢測在新生兒的應用。陳菁兒醫師說明,上圖中藍色圈圈代表由新生兒聽力篩檢所發現當下已經有嚴重聽損的寶寶,橘色圈圈是利用基因檢測所找出來較輕微、以及晚發型的聽損寶寶。研究發現這兩種檢查重疊的部分很小,也就是說新生兒基因檢測可以找到傳統聽力篩檢無法篩檢到的族群,且兩者同等重要,無法互相取代。這樣的研究開啟了新生兒基因篩檢的應用,在台灣也已經頗為普及,準父母在產檢過程中都可以由醫療院所獲得相關資訊。《麻醉風暴》上演的惡性高熱 檢測有助日後用藥安全不同檢測技術,可以找出的不同疾病特性的族群,陳菁兒醫師說明,新生兒代謝篩檢採檢當下寶寶血液中的代謝物質,可以偵測出急性且嚴重的代謝疾病,但輕型或晚發型代謝疾病就不一定驗得出來;新生兒基因檢測則可以提早找出高風險寶寶,後續便能加強照護和追蹤。除了聽力損傷及代謝疾病,目前新生兒基因檢測的應用範圍很廣,還可以進階到找出特定中樞神經、血液、肌肉、心臟、視力等多種疾病,陳菁兒醫師說,透過基因檢測甚至可以了解一些藥物過敏的問題。「基因檢測可以實現預防醫學與精準醫療的概念。」陳菁兒醫師說,以藥物過敏為例,輕微的可能只是皮膚搔癢紅腫,但嚴重可能導致死亡。過去大家只能在用藥之後,才從臨床反應知道是否對藥物過敏,現在則可利用藥物基因檢測找出可能引起過敏反應的藥物,就醫時就能提醒醫師避免使用相關藥物,或調整藥物劑量,以降低藥物不良反應發生的機會。藥物基因體學包括藥物代謝與藥物不良反應的資訊,陳菁兒醫師分析,因為每個人對藥物代謝的速率不同,所以在相同劑量下可能產生不同的反應,譬如小朋友常用的退燒藥,可能因為代謝速率不同而導致不良反應,嚴重可能造成腸胃道出血。成人常用的降尿酸藥物,在某些人身上可能出現史帝芬強生症候群(Steven-Johnson Syndrome,SJS)或毒性上皮溶解症(Toxic Epidermal Necrolysis,TEN),皮膚會嚴重潰爛,甚至導致死亡。還有知名電視劇《麻醉風暴》中上演的惡性高熱,主要是因為帶有特殊基因的人群,在使用某些麻醉藥物後容易演變成惡性高熱,而危及性命。陳菁兒醫師說,以往這些比較特殊的案例,常找不到原因,但是現在透過藥物基因檢測,我們可以提早找出容易對這些高敏感藥物產生不良反應的族群,有助於提升用藥安全。因為人體的遺傳基因不會改變,一輩子只需要驗一次即可,這些攸關用藥安全的資訊,長大以後也都非常實用。基因檢測讓家族成員連帶受益針對有家族史的寶寶,因為帶有相同疾病基因變異的機率比較高,需要以基因檢測確認是否為高風險寶寶,提早做預防照護。至於沒有家族史的寶寶,則可以透過基因檢測找出相關疾病,並能藉此找出隱藏的家族史而讓整個家族受益。也就是說,新生兒基因檢測的好處其實不只侷限在受檢的寶寶,包含已出生、未出生的兄弟姊妹、其他家族成員,甚至上一代或下一代都可能是受益的對象。無論是否有已知家族史,如果新生兒驗出疾病基因變異,都應該接受完整遺傳諮詢,必要時再進行相對應基因檢測。「有的家族因為寶寶做了基因檢測,才發現其他家族成員其實也有相同的疾病,因而得以提早接受治療。」陳菁兒醫師說,了解遺傳疾病的狀況,也可以讓爸爸媽媽在準備生育下一胎時,做好計畫。貼心小叮嚀陳菁兒醫師提醒,基因檢測是一種風險評估的概念,一生只需驗一次,就可以得到終身受用的基因疾病資訊。提早檢測就越能夠提早預防,避免錯失疾病的黃金治療期,甚至其他家族成員也可能連帶受益。(文章授權提供/照護線上)
(優活健康網新聞部/綜合報導)小朋友會罹癌嗎?據中華民國兒童癌症基金會統計,台灣一天約有1.5個兒童罹癌。由於兒童無法清楚地表達身體異狀,因此常在發病晚期才發現,導致錯過治療的黃金時機而終身遺憾。兒童專科診所吳俊厚院長表示,配合國健署新生兒疾病篩檢以及基因檢測,雙管齊下效果會更佳,可以及早治癒或減緩嚴重症狀的產生。每天1.5名兒童罹癌 血癌發生率最高成人常見的癌症如大腸癌、乳癌及肺癌等,多為後天因素所致;兒童癌症成因較多為自身體質與基因的關係,有可能是遺傳父母親致癌基因或是媽媽在懷孕過程發生基因突變,導致新生兒罹癌。中華民國兒童癌症基金會統計資料顯示,台灣兒童癌症發生率最高為血癌(34.9%),其次依序為中樞神經瘤(20.1%)、淋巴瘤(9.2%)、骨肉瘤(7%)、神經母細胞瘤(6.2%)等。兒童癌症難以被發現,當小朋友身體不舒服時,往往只能以哭鬧來表現,無法描述自己不舒服。發現罹癌時,往往已經來不及,因此家長的警覺性很重要,留意到子女有任何異狀需立即求醫。摘眼球保命 學習社交皆遭遇瓶頸曉馨2歲時,因感冒到醫院看診,醫護人員注意到她的雙眼瞳孔隱約有白色反光,看起來像貓眼一樣,到眼科檢查後診斷為視網膜母細胞瘤。由於腫瘤發展迅速,曉馨的爸爸媽媽即使百般不願意,也只能忍痛同意醫師摘除較嚴重的左眼,換上義眼取代,而右眼則透過化學治療控制腫瘤。雖然曉馨的視力保住了,但是學習變得吃力,在社交上也遇到瓶頸,甚至要承受別人異樣的眼光。兒童專科診所吳俊厚院長表示,視網膜母細胞瘤越早發現,治療效果越佳。視網膜母細胞瘤在胚胎時期就已產生病變,但表徵不明顯,多數患者確診時已是晚期,須摘除眼球保命。類似的基因缺陷會給小朋友成長過程帶來不可逆的影響。新生兒疾病篩檢、基因檢測可雙管齊下吳俊厚院長表示,曾遇過父母因為大寶小小年紀罹癌,不希望同樣的事情發生在二寶身上而諮詢基因檢測的案例。雖然現在藥物和治療技術進步,兒童癌症的治療成功機率較成人高出許多,若能透過基因檢測發現疾病,就可以及早治癒或減緩嚴重症狀的產生。台灣大學基因體暨蛋白體醫學研究所博士洪加政表示,新生兒基因檢測只需少量血,就可檢測208個基因、200種疾病,含 8種過去難以檢測出的罕見小兒癌症。吳俊厚院長提醒,國健署新生兒疾病篩檢與基因檢測雙管齊下,可多一份安心。若孩子已經出現明顯症狀,亦可透過基因檢測找到病因,希望新手爸媽們不要害怕知道孩子身體狀況,及早發現,及早治療。(文章授權提供/健康醫療網)
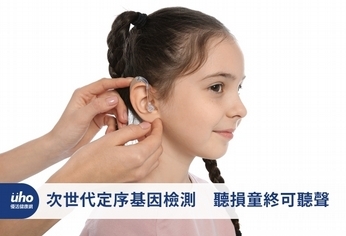
(優活健康網新聞部/綜合報導)臺大醫院推動「次世代定序」基因檢測,結合基因醫學部與耳鼻喉部的醫療專業,攜手國家實驗研究院國家高速網路與計算中心(國研院國網中心)、科技部生命科學研究發展司生技醫藥核心設施平台,以及國家衛生研究院亞太生醫矽谷精準醫療旗艦計畫之次世代基因體分析平台,可以從人體的2萬多個基因中,抽絲剝繭找尋出重要的聽損基因,並透過臺灣AI雲(TWCC)分析及加速的效果,幫助聽損兒童把握黃金治療期,重獲新「聲」。每年超過700位聽損童需接受治療聽力是語言、學習、溝通交流的重要接收能力,在新式的聽損基因檢測工具出現前,先天性聽損兒童有70%找不出聽損原因,往往導致臨床決策及遺傳諮詢上的困難,也常使得一些聽損兒童錯過了治療黃金期。依據國民健康署統計,新生兒先天性聽力損失的發生率約為3‰至4‰,每年有超過700位聽損兒童需要接受進一步治療。國研院國網中心與臺大醫院合作,提供為期3年百萬核心運算小時數的臺灣AI雲計算資源,以及整合儲存及定序流程的整體服務方案,相當於提供1,000位以上聽損兒童診斷分析的計算資源,讓檢測的過程加速4~6倍,協助醫師做出最佳的診斷和治療,讓超級電腦的加速,轉化成聽得見的進步。讓每位等待曙光的家長和孩子,感受到冬天傳來的溫暖與希望。國研院國網中心的次世代基因體分析平台,提供次世代基因體分析軟體與資料庫比對服務,且涵蓋生醫巨量資料分析所需要的大記憶體及平行計算設備、結合定序後產生大型檔案傳輸與儲存計算所需要的高速平行化檔案系統,同時提供異地備份設施服務以保存重要的定序資料,可以滿足研究和實務之需求。隨著醫療現代化的發展,輕、中度聽損的病人可使用助聽器,幫助放大外界的音量,而內耳耳蝸受損的重度和極重度聽損者,則可評估植入人工電子耳,藉由電極傳遞訊息,直接刺激聽神經而產生聽覺。然而並不是每個重度聽損病人接受人工電子耳手術皆能獲得良好成效,手術前的審慎評估和手術後的復健是人工電子耳手術成功的必要條件。透過基因檢測的方式,可以協助醫師評估使用最適當的聽損矯治輔具,讓聽損兒童及早接受適當的矯治,迎接幸福的人生。
(優活健康網編輯部/綜合整理)標靶治療最早的藥是基立克(Glivec),在慢性白血費城染色體上發現的重組基因Bcr-Abl 蛋白發展出來的酪氨酸激脢受體抑制劑,一開始的臨床試驗就有驚人的療效,徹底顛覆了標靶藥對比化療的差別,2001 年通過美國食品藥物管理局審批後,各類靶向藥就如雨後春筍般的出現。幾個重要的基因相對應的藥物已徹底的改變了癌病治療的觀念和手段。次世代的基因檢測技術(NGS)發展快速,能快速地全基因解碼,透過大數據分析,全面的了解可能可以用的藥物。生物標記包括了預後判斷(生存期相關)或預測判斷(可能對某藥物的有效性)的指標,由於是個人的基因,當然也可以說是個人化的精準醫學。除了昂貴的基因解碼最為詳細與準確外,事實上,醫院透過傳統的病理切片,以組織染色法已能粗略並快速地找出合適的藥物,如乳癌常見的(約20%~30%) Her2 指標,肺癌的ALK,胃腸道基底癌GIST 的C-KIT 以及免疫治療常用的PD-L1,若是為了更進一步了解特定基因更細膩的突變點,就須借助基因檢測,將EGFR、ALK、Braf、C-KIT 常見的位點做進一步的了解,其實,單一基因特定藥物由有效變成無效常常是因為又有新的突變點發生。由於基因變異遠比拿得到的藥多,所以如果為了找已知的那幾種標靶藥而做基因檢測,常常不見得加分,反而是找治療策略較有意義。針對一系列,最多十至卅個預後相關的基因做檢測,給予一個基因表達分數,做為臨床醫師是否據以推薦該治療的指引,例如檢驗21 個基因,用在早期荷爾蒙陽性淋巴結未轉移的乳癌是否需要化療的參考;或是用來指導攝護腺癌手術後是否還需要追加放射治療等的決策參考,都有商品化產品,這種檢測似乎比較有用。由於「次世代基因檢測」技術大量篩出上百個基因突變點,這些突變就算是生物學上有意義,目前臨床上能用上藥的並不多,約在20%之間。另外還有些疾病是決定於基因的表現(徵),即使沒有DNA突變,由於包覆在基因外面的蛋白結構甲基化,磷酸化或去乙醯化,影響蛋白質生成的轉譯動作,讓蛋白質不表達,一樣是重大的影響功能,但基因檢測不一定做出結果來,所以是否需在疾病早期就以基因檢測做為用藥指引的手段,目前許多研究還在進行中,尚未有定論。總之,基因檢測針對獨特的基因缺陷而設計出來的藥物就是精準醫學的意義,但是,因為醫療經濟效益不夠高以及藥物發展不夠快,想要全面的應用還不太可能。例行性的做NGS,少部分的人可以從中找到藥,但若想要全面性都做,即使大型醫院或保險公司也無法例行的做此事。(本文摘自/自己的癌症自己救/時報出版)
地址:台北市中山區長春路328號7樓之2
廣告合作:[email protected]
廣告合作:[email protected]
Copyright © www.uho.com.tw All Rights Reserved By 優活健康股份有限公司
Menu